発表概要
【ポイント】
- ヒト胚着床を培養皿上で再現できる胎児-母体アセンブロイド(注1)を創出し、ヒト胚着床機序を解明するためのプラットフォームを作製しました。
- このプラットフォームを用いて、着床過程の各段階を再現することに成功し、胎盤の細胞と母体の細胞が融合し得ることを世界で初めて示しました。
- 着床不全(注2)、周産期疾患、子宮内膜症や子宮体癌の病態解明や予防法および治療法の開発への応用が期待されます。
着床は妊娠成立において最初の重要なステップですが、ヒト着床機序を研究するための適切なモデルがありませんでした。
東北大学大学院医学系研究科情報遺伝学分野と周産期医学分野、熊本大学発生医学研究所胎盤発生分野、東京大学定量生命科学研究所大規模生命情報解析研究分野、東京医科歯科大学生体材料工学研究所診断治療システム医工学分野らの研究グループは、ヒト子宮内膜(注3)細胞を用いて生体子宮内膜組織と空間的配置や構成細胞が類似した子宮内膜オルガノイド(注4)モデルの作製に成功しました。また、このモデルとヒト胚性幹(ES)細胞を用いて、胚着床を培養皿上で再現する胎児-母体アセンブロイドを世界で初めて作成し、着床の各段階を再現することに成功しました。さらに、ヒト胚から派生する胎盤細胞と子宮内膜間質細胞が融合することを確認し、着床過程で胎盤の細胞と母体の細胞が融合し得ることを世界で初めて示しました。本研究成果は、着床の瞬間を視覚化する新たなモデルとして、着床機序の解明や不妊治療法の開発のための有用なプラットフォームとなることが期待されます。
本研究成果は、日本時間2024年2月24日(土)午前4時(米国東部時間2月23日(金)午後2時)に科学誌Science Advances誌に掲載されました。
詳細な説明
【研究の背景】
近年、我が国をはじめ欧米先進諸国では、晩婚化や女性の社会進出などの社会情勢を背景に、出生数の減少が進んでいます。そのため、体外受精や顕微授精などの生殖補助医療(ART)は、少子化対策の重要な手段となっています。しかし、ARTの移植胚の着床率は依然として低く、なかでも形質良好胚を繰り返し移植しても妊娠に至らず、治療を諦める難治性着床不全の症例数が多数存在し、解決すべき重要課題となっています。着床不全の改善のためには、胚着床過程における胎児と母体間の相互作用について理解することが重要です。
着床機序は動物種によって多様であり、特にヒト胚は、子宮内膜に深く侵入するなどの特徴があります。そのため、マウス等の動物モデルにおける知見をヒト着床機構に当てはめることは困難です。また、ヒト胚の着床期の観察や解析は、技術的・倫理的に不可能なため、ヒト胚着床機構の理解のためには、培養皿上で観察できるin vitroモデルの利用が重要です。近年、多能性幹細胞から着床前の胚である胚盤胞様の構造(ブラストイド)(注5)が誘導できることが報告され、注目されています。また、母体側の子宮内膜細胞は、オルガノイド技術により長期維持が可能となり、疾患の模倣などが試みられています。しかし、従来の子宮内膜オルガノイドは、嚢胞状(シスト)の構造を取り、胚が接着する側である頂端(アピカル)面が、培養基質の内部に埋没しているため、着床研究への利用が困難でした。
【今回の取り組み】
東北大学大学院医学系研究科情報遺伝学分野の柴田峻助教、有馬隆博名誉教授、周産期医学分野の遠藤俊大学院生、齋藤昌利教授、熊本大学発生医学研究所胎盤発生分野の岡江寛明教授、東京大学定量生命科学研究所大規模生命情報解析研究分野の中戸隆一郎准教授、東京医科歯科大学生体材料工学研究所診断治療システム医工学分野の梶弘和教授らの共同研究グループは、子宮内膜上皮と間質細胞、さらに血管内皮細胞を混合培養することにより、子宮内膜上皮の頂端面が外側に露出し、間質細胞と血管網を内包する子宮内膜オルガノイドモデル(アピカルアウト-子宮内膜オルガノイド)を作製しました(図1)。この新しいオルガノイドモデルは、ホルモン添加時に従来のオルガノイドよりも高度な成熟化を示しました。また、シングルセル遺伝子発現解析や生体(in vivo)の遺伝子発現データとの統合解析により、生体との類似度も確認しました。さらに、この子宮内膜モデルにナイーブ型ES細胞より誘導した胚盤胞様構造(ブラストイド)を加えることで、胚着床を再現するin vitroモデル(胎児-母体アセンブロイド)の作製にも世界で初めて成功しました(図2・3)。この胎児-母体アセンブロイドは対位・接着・浸潤とよばれる過程を含む着床の各段階を再現し、胚から派生した胎盤細胞の一種である合胞体栄養膜細胞によって、子宮内膜上皮細胞が破られることを確認しました。また、合胞体細胞は、子宮内膜間質細胞に向かい浸潤し、最終的には子宮内膜間質細胞と融合することを世界で初めて明らかにしました。
【今後の展開】
本研究の成果は、着床時の初期胚と母体の相互作用を調べるための基礎となり、着床不全の治療や生殖補助医療の進歩に貢献し得る貴重な知見を提供するものです。また、本モデル(図4)を応用し、胎盤組織(栄養膜細胞など)と母体組織(子宮内膜)の相互作用の知見を深めることで、着床不全や周産期疾患の発症予測・予防や治療法の開発につながることが期待できます。さらに、子宮内膜症や子宮体癌の病態解明や治療法、予防法の開発への応用も期待できます。
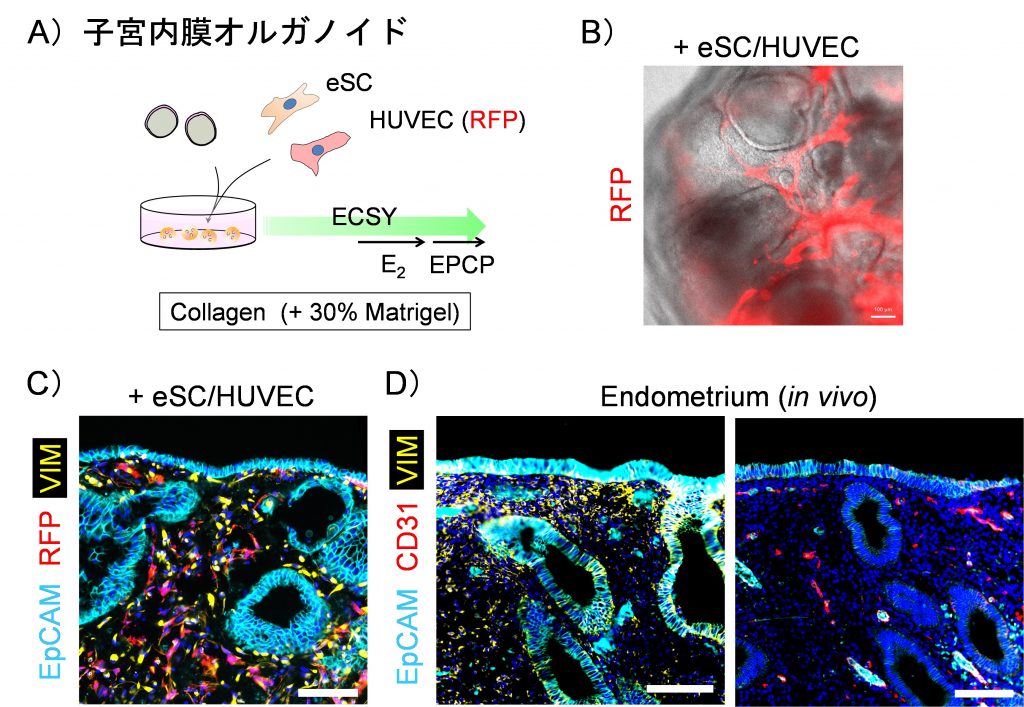
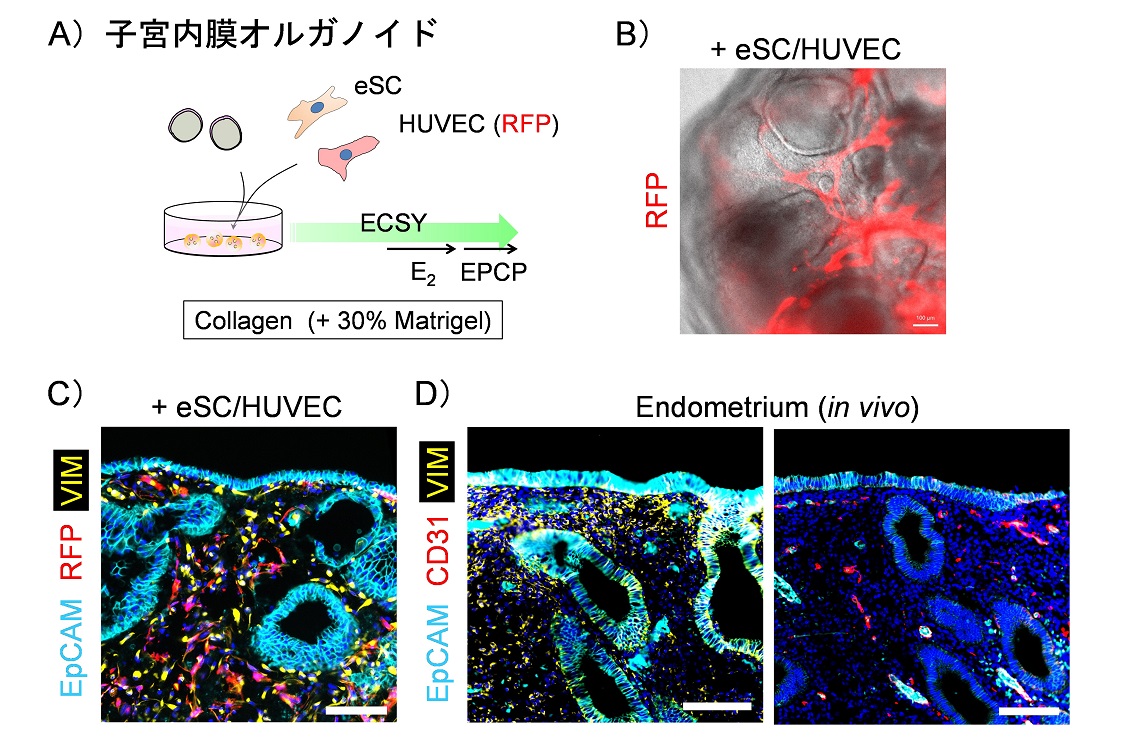
図1. 子宮内膜オルガノイドモデル
(A)子宮内膜オルガノイドモデル内への血管内皮細胞の共培養手順の概略を図に示す。(B)子宮内膜モデル内の血管内皮細胞のネットワーク構築の様子。子宮内膜間質細胞(eSC)とHUVECを含む子宮内膜オルガノイドモデルの明視野と蛍光像。スケールバー、500μm。(C, D)子宮内膜オルガノイドモデル。(C)と生体のヒト子宮内膜組織(D)をEpCAM、CD31、VIMで染色した蛍光像;核はHoechst(青)で染色。スケールバー、100μm。
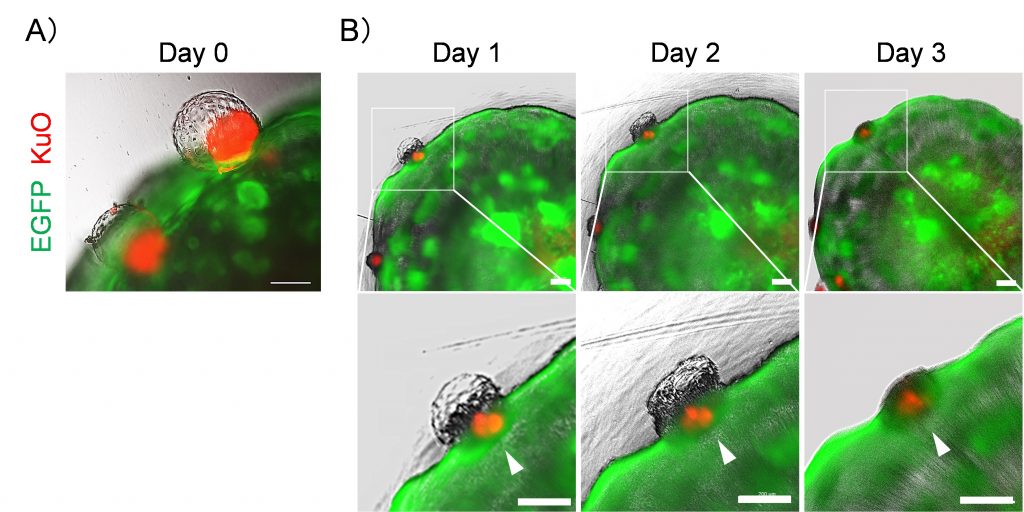
図2. ブラストイドの子宮内膜モデルへの着床
(A)ブラストイドは、実際のヒト胚と同じ様式で、内部細胞塊(ICM)側から子宮内膜オルガノイドモデルに対向配置され付着している。(B)1、2、3日目のヒトブラストイド(オレンジ)とアピカルアウト-子宮内膜オルガノイド(AO-EMO、緑)の明視野像と蛍光像。矢印はブラストイドを示す。スケールバー、200 µm。ヒトブラストイドと子宮内膜オルガノイドモデルの共培養を続けると、ブラストイドは子宮内膜モデルに接着し、内部に入り込むように扁平化した。
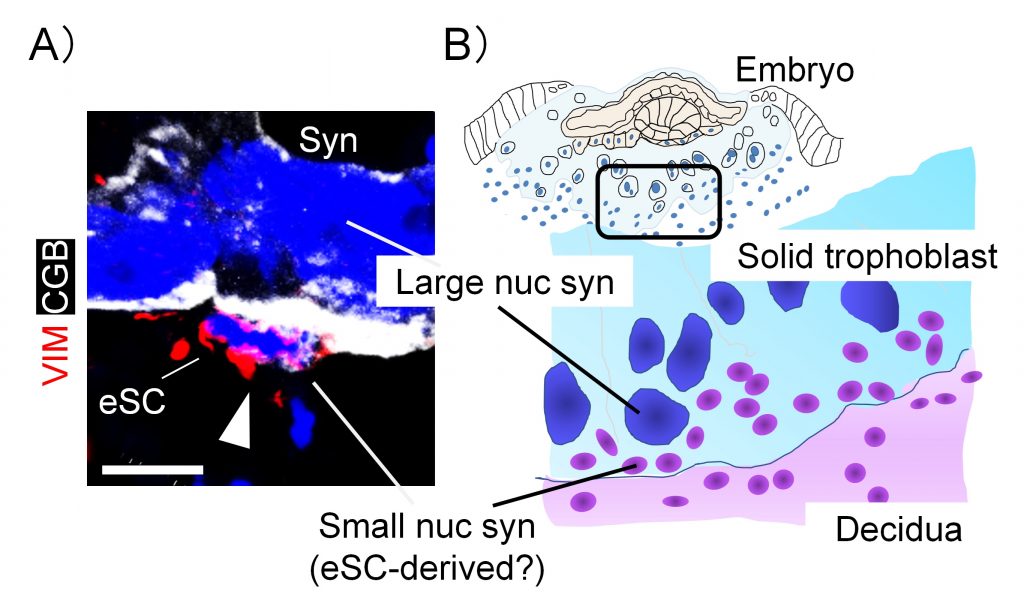
図3. 胎児-母体アセンブロイドの創出
(A)子宮内膜間質細胞マーカーVIMと合胞体細胞マーカーCGBで染色した母体-胎児アセンブロイドの代表図;核はヘキスト(青)で染色。矢印はVIM+/CGB+細胞を示す。スケールバー、50μm。大きな核を持つ合胞体細胞のこのような浸潤は、胎時児-母体界面における胚の着床時に観察される原始合胞体の構造と類似する。(B)ヒト胚の着床と脱落膜への浸潤の模式図。原始合胞体と間質細胞の界面では、大きな核と複数の小さな核から成る特徴的な合胞体(solid trophoblast)が形成される。
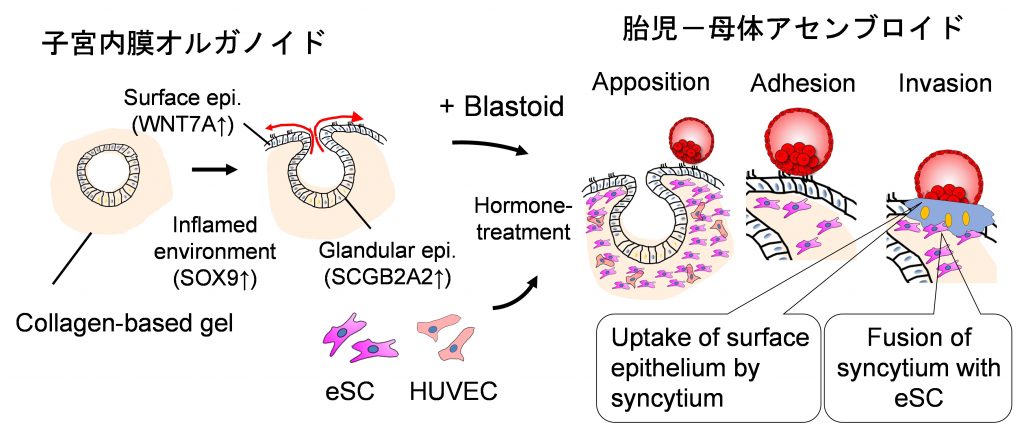
図4. ヒト胚と子宮内膜における融合現象
子宮内膜上皮は、コラーゲンゲルを用いることにより管腔面を外側に露出し、管腔上皮・腺上皮に分化する。さらに、子宮内膜間質細胞(eSC)とヒト臍帯静脈内皮細胞(HUVEC)を混合することで作製した3Dヒト子宮内膜モデルに、ヒトブラストイドを共培養することで、ヒト胚着床を再現した。ブラストイドから派生した合胞体栄養膜細胞は、子宮内膜上皮のバリアを破り、更に子宮内膜間質細胞と融合することで子宮内膜内に浸潤を進めるという着床の進行・胎盤発生のメカニズムが示唆された。
謝辞
本研究は、文部科学省科学研究費補助金(課題番号:JP21H04834, JP21K15098)、国立研究開発法人日本医療研究開発機構(AMED)革新的先端研究開発支援事業(AMED-CREST)(課題番号:JP19gm1310001)、国立研究開発法人日本医療研究開発機構(AMED)再生医療実現拠点ネットワークプログラム(課題番号:JP21bm0704068)、国立研究開発法人日本医療研究開発機構(AMED)成育疾患克服等総合研究事業(Birthday)(課題番号:JP23gn0110072)、公益財団法人武田科学振興財団、公益財団法人内藤記念科学振興財団等の支援を受けて行われました。
用語説明
注1.胎児-母体アセンブロイド:胚盤胞様構造物(ブラストイド)と子宮内膜オルガノイドの集合体モデル。
注2.着床不全:着床不全は受精卵が女性の子宮内膜に正常に着床しない状態を指します。着床不全の原因は多岐にわたり、ホルモンバランスの乱れ、子宮内膜の異常、免疫学的要因、さらには生活習慣や環境要因などが関与すると考えられています。着床不全は、特に体外受精を試みるカップルにとって重要な課題であり、着床不全の理解を深めることは、不妊の課題に対処し、生殖補助医療技術(ART)を向上させる上で非常に重要であるといえます。
注3.子宮内膜:子宮の最外層にあり、月経周期と妊娠において重要な役割を果たします。子宮内膜は、上皮細胞、間質細胞、血管、免疫細胞などの細胞から構成され、ホルモンの変動に応じて劇的に変化する組織です。月経周期は増殖期、分泌期、月経期からなり、それぞれが子宮内膜に異なる影響を及ぼします。ホルモンの上昇により、子宮内膜は、血管が増加し分厚くなり、胚の着床に備えます。子宮内膜の発育に異常があると、不妊症、子宮内膜症、異常子宮出血などの症状を引き起こします。
注4.オルガノイド:幹細胞や組織幹細胞から作り出された三次元のミニチュア臓器様構造です。オルガノイドは、三次元構造を持ち、実際の臓器の主要な機能や特徴を再現することが可能であり、臓器の発生、疾患の病理学、薬剤評価など、多様な研究用途を有する貴重なモデルとなっています。
注5.胚盤胞様構造物(ブラストイド):ヒトの初期段階の胚である胚盤胞(blastocyst)を模倣した、実験室で細胞から作製される人工的な構造です。ブラストイドは、主にナイーブ型といわれる着床前の胚に相当するヒト多能性幹細胞を、浮遊培養と特定の培地などの培養環境で誘導することによって作製されます。実際の胚を用いることなく、ヒトの初期発生を研究できる貴重な資源となっています。
アイキャッチ画像
雑誌名等
雑誌名:Science Advances
論文タイトル:Modeling Embryo–Endometrial Interface Recapitulating Human Embryo Implantation
著者:Shun Shibata*, Shun Endo, Luis A. E. Nagai, Eri H. Kobayashi, Akira Oike, Norio Kobayashi, Akane Kitamura, Takeshi Hori, Yuji Nashimoto, Ryuichiro Nakato, Hirotaka Hamada, Hirokazu Kaji, Chie Kikutake, Mikita Suyama, Masatoshi Saito, Nobuo Yaegashi, Hiroaki Okae, & Takahiro Arima*
*責任著者:東北大学大学院医学系研究科情報遺伝学分野
助教 柴田 峻(しばた しゅん)、名誉教授 有馬 隆博(ありま たかひろ)
問い合わせ先
(研究に関すること)
東北大学大学院医学系研究科情報遺伝学分野
助教 柴田 峻(しばた しゅん)
TEL:022-717-7844
Email: shun.shibata.a3[@]tohoku.ac.jp
名誉教授 有馬 隆博(ありま たかひろ)
TEL:022-717-7844
Email:tarima[@]med.tohoku.ac.jp
(取材に関すること)
東北大学大学院医学系研究科・医学部広報室
東北大学病院広報室
TEL:022-717-8032
FAX:022-717-8931
Email:press[@]pr.med.tohoku.ac.jp
熊本大学総務部総務課広報戦略室
TEL:096-342-3269
FAX:096-342-3110
Email:sos-koho[@]jimu.kumamoto-u.ac.jp
東京大学定量生命科学研究所総務チーム
TEL:03-5841-7813
Email:soumu[@]iqb.u-tokyo.ac.jp
東京医科歯科大学総務部総務秘書課広報係
TEL:03-5803-5833
Email:kouhou.adm[@]tmd.ac.jp
※メール送信時は[@]を半角の@に置き換えてください。