
|
肝臓の発生 -肝構成細胞とその相互作用-
各画像はクリックで拡大します。
マウスにおける肝臓の発生は、胎齢8.5日頃に腹側の前腸内胚葉が心臓中胚葉からのFibroblast growth factor(FGF)シグナルと、横中隔間充織からのBone morphogenic protein(BMP)シグナルの刺激により肝芽を形成することから始まる。肝芽を構成する肝芽細胞は、胎児肝における組織幹細胞であり、Hepatocyte growth factor(HGF)、Transforming growth factor β(TGFβ)、Wntなどの種々のシグナルを受け増殖する。(図1)
胎齢10日前後になると、造血系の細胞が大動脈・性腺・中腎領域(aorta-gonad-mesonephros region ; AGM領域)及び胎盤より流入し、肝臓は造血器官として機能するようになる。この間に、非実質細胞が産生するHGFや種々の細胞外基質が、肝芽細胞の肝実質細胞への分化を促進することが明らかになっている。その後、肝臓は胎児の主要な造血器官として機能するが、出生前後に造血の場は肝臓より骨髄へと移行し、肝臓は代謝器官へと分化していく。
我々は、このように様々な細胞の間の相互作用によって制御されている肝発生について、(1)マーカー分子の同定による各種肝臓構成細胞の解析と(2)サイトカインを中心とした細胞間シグナル伝達機構の解析という、2つの観点から研究を進めている。
|
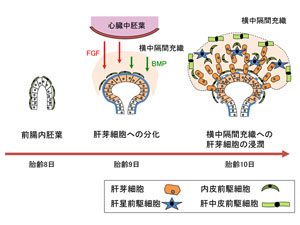
図1 マウスにおける肝臓の発生 |
マーカー分子の同定による各種肝臓構成細胞の解析
当研究室では、胎児期の未分化な肝臓構成細胞を分離・同定するための多くのマーカー分子をクローニングしてきた。その1つが、肝芽細胞に発現しているDlk/Pref-1(以後Dlkとする)である。Dlkに対する抗体を用いることにより、胎児肝臓からDlk陽性の肝芽細胞を効率良く分離することができる。分離した肝芽細胞はin vitroで培養が可能であり、培養条件により肝実質細胞及び胆管上皮細胞に分化することが可能である(図2、Tanimizu N, J. Cell Sci. 2003, Tanimizu N, J. Cell Sci. 2004)。また、Dlk以外にもp75NTR(肝星細胞および門脈域線維芽細胞)、PCLP-1(肝中皮細胞)、Stab2(肝類洞内皮細胞)、Lyve-1(肝類洞内皮細胞)などの分子も見出した(図3、Suzuki K, Gastroenterology 2008, Onitsuka I, Gastroenterology 2010, Nonaka H, Dev. Dyn. 2007)。これらの分子に対する抗体を作製し、セルソーターにより様々な分化段階の肝臓構成細胞を分取することが可能となったことから、肝発生のメカニズムが細胞レベルで明らかになりつつある(図4)。現在、単独培養による各種細胞の分化機構の解析や、共培養による異なる細胞種間の相互作用の機構の解析を進めている。
さらに、これらマーカー分子のプロモーターを利用し、細胞種特異的にCreを発現するマウスの作製も進めている。このマウスを利用し、細胞種特異的なノックアウトマウスの作製や細胞系譜の標識による解析も行おうとしている。
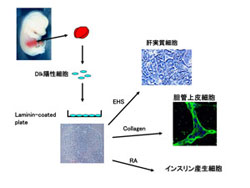
図2 Dlk陽性細胞
|
 |
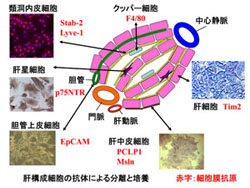
図3 肝構成細胞と細胞膜抗原分子
|
 |
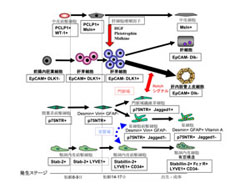
図4 肝臓構成細胞の分化系譜と
肝形成における細胞間相互作用モデル |
サイトカインを中心とした細胞間シグナル伝達機構の解析
当研究室では、サイトカイン、特にIL-6ファミリーのサイトカインであるOncostatin M(OSM)に注目して解析を進めてきた(図5)。OSMは1986年にヒトのメラノーマ(黒色腫)細胞株の増殖を抑制する因子として同定された。我々は、マウスOSM をクローニングし、肝芽細胞の肝実質細胞への分化は血液細胞が産生するOncostatin M (OSM)が促進していることを見出した(Kamiya A, EMBO J 1999)。また、OSM受容体サブユニットをクローニングし、OSM受容体のノックアウトマウスの作製を行った(Minehata K, Int. J Hematol. 2006, Esashi E, Eur. J Immunol. 2009, Tanaka M, Blood 2003)。現在、OSM受容体ノックアウトマウス及びOSMノックアウトマウスを用いて、OSMの生体における機能の解析を進めている。
また、前述の肝臓構成細胞を分離・培養する技術を利用した、肝臓の発生・分化を制御するシグナルに関しても解析を進めている。例えば、Dlk陽性である肝芽細胞の培養系を用いて、NotchシグナルやHedgehogシグナルがそれぞれ胆管の発生や肝実質細胞分化に重要な因子であることを示した(Tanimizu N, J Cell Sci. 2004, Hirose Y, Exp. Cell Res. 2009)。また、Dlk自身の生体における機能の解析も行っており、今までは機能未知であったDlkは、CfrというFGF受容体を介してFGFシグナル系の制御を行っているということも突き止めた(Miyaoka Y, Development 2010)。
|
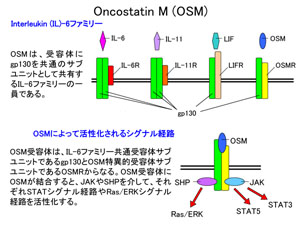
図5 OSMシグナル |
|

|